Pressione di vapore: nozioni di base ed esempi
Introduzione: Che cos'è la tensione di vapore?
La tensione di vapore è un termine cruciale della termodinamica e della chimica fisica che descrive la pressione di equilibrio di un vapore rispetto alla sua forma liquida o solida a una determinata temperatura. Ci dice semplicemente quanto facilmente una sostanza evapora. Un liquido a rapida evaporazione ha un'alta pressione di vapore (ad esempio, l'acetone), mentre un liquido a lenta evaporazione ha una bassa pressione di vapore (ad esempio, il mercurio).
Come funziona la tensione di vapore
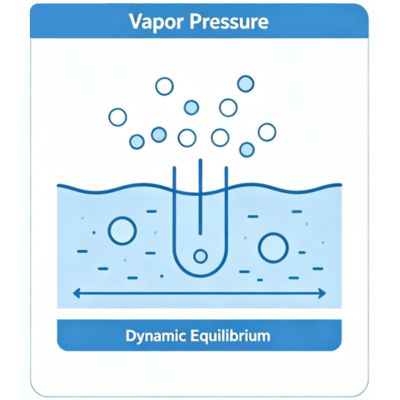
A qualsiasi temperatura, alcune molecole di un liquido hanno un'energia cinetica sufficiente per evaporare nella fase di vapore. Sempre più molecole evaporano e alcune ritornano nel processo di condensazione. Nella fase in cui il tasso di evaporazione è uguale al tasso di condensazione, il sistema è in equilibrio: la pressione di vapore alla data temperatura è descritta da questo equilibrio. La dipendenza esponenziale della pressione di vapore dalla temperatura deriva dall'equazione di Clausius-Clapeyron.
Fattori che influenzano la pressione di vapore
1. La temperatura
La temperatura ha l'effetto più diretto sulla pressione di vapore. Con l'aumento della temperatura, l'energia cinetica delle molecole aumenta e più molecole possono uscire dalla fase liquida. Ad esempio, la pressione del vapore acqueo aumenta da 17,5 mmHg a 20°C a 760 mmHg a 100°C, dove bolle alla pressione atmosferica standard.
2. Forze intermolecolari
Maggiori forze intermolecolari, come il legame a idrogeno o le forze di van der Waals, riducono la pressione del vapore. L'acqua con legame a idrogeno ha una pressione di vapore molto più bassa rispetto all'acetone con debole interazione dipolo-dipolo.
3. Natura della sostanza
Anche la forma della molecola è importante. Le sostanze con molecole più leggere e meno polari (etere dietilico) hanno pressioni di vapore più elevate di quelle più pesanti o con legami più forti (glicerolo o mercurio).
Metodi di misurazione della tensione di vapore
1. Metodo manometrico
È la tecnica classica in cui il liquido è contenuto in un recipiente sigillato e la pressione di vapore all'equilibrio viene misurata direttamente con un manometro dopo il raggiungimento dell'equilibrio. Fornisce letture accurate a pressioni da basse a moderate.
2. Metodo dinamico
Questo metodo quantifica la pressione di vapore dalla variazione del volume o del peso del liquido nel tempo, quando il vapore viene rilasciato. Si applica soprattutto a sostanze che evaporano rapidamente o a temperature elevate.
3. Metodo dell'effusione
Il numero di molecole di gas che escono attraverso un piccolo poro (effusione) varia linearmente con la pressione del vapore. È adatto a campioni minuti e a sostanze volatili.
4. Calcoli di Clausius-Clapeyron
Per la maggior parte delle sostanze, la misurazione diretta non è possibile. La pressione di vapore a varie temperature viene quindi determinata dall'equazione di Clausius-Clapeyron sulla base dei punti di ebollizione e dell'entalpia di vaporizzazione determinati sperimentalmente.
Significato pratico della tensione di vapore
1. Meteorologia e climatologia
Lapressione di vapore è direttamente correlata all'umidità, un parametro fondamentale per le previsioni meteorologiche e le precipitazioni. Ad esempio, l'umidità relativa (RH) è il rapporto tra la pressione del vapore acqueo effettivo e la pressione del vapore di saturazione a una determinata temperatura. La misurazione accurata della pressione del vapore aiuta a prevedere i punti di rugiada, la nebbia e le precipitazioni.
2. Ingegneria industriale e chimica
Nella pressione di vapore, nell'evaporazione e nella separazione chimica, la pressione di vapore determina il comportamento degli oggetti in caso di riscaldamento e raffreddamento. La raffinazione del petrolio, ad esempio, dipende dalle differenze di pressione del vapore per separare idrocarburi come l'esano e il toluene mediante distillazione frazionata.
Nella refrigerazione, i refrigeranti come l'R134a o l'ammoniaca vengono scelti in parte per le loro proprietà di pressione di vapore: devono evaporare e condensare bene entro un intervallo di pressioni sicuro.
3. Applicazioni farmaceutiche
Le formulazioni di farmaci contenenti componenti volatili devono tenere conto della pressione di vapore per garantire la stabilità e la durata di conservazione. Ad esempio, i gel antisettici a base di etanolo utilizzano formulazioni con pressioni di vapore controllate per bilanciare l'efficacia e la velocità di evaporazione.
4. Scienza ambientale
La pressione di vapore determina anche il comportamento dei contaminanti, come i composti organici volatili (COV), nell'atmosfera. I composti ad alta pressione di vapore, come il benzene o l'acetone, contribuiscono in modo significativo alla formazione dello smog e sono sottoposti a forti controlli nell'ambiente.
Esempi e dati
|
Sostanza |
Pressione di vapore a 20°C (mmHg) |
Pressione di vapore a 100°C (mmHg) |
|
Acqua |
17.5 |
760 |
|
Etanolo |
44.6 |
400 |
|
Acetone |
180 |
760 |
|
Metanolo |
95.3 |
1300 |
|
Benzene |
75.1 |
450 |
|
Etere dietilico |
430 |
5800 |
|
Mercurio |
0.0012 |
0.2 |
|
Esano |
150 |
450 |
|
Toluene |
22.3 |
230 |
|
Cloroformio |
160 |
500 |
Queste figure illustrano come le forze molecolari e la temperatura influenzino la volatilità. L'etere dietilico, ad esempio, bolle molto rapidamente a temperatura ambiente a causa della sua elevata pressione di vapore, mentre il mercurio si avvicina alla non volatilità anche a temperature elevate. Per ulteriori informazioni, consultare Stanford Advanced Materials (SAM).
Domande frequenti
Che cos'è la pressione di vapore?
La pressione di vapore è la pressione di un vapore in equilibrio con il suo liquido o solido a una determinata temperatura.
In che modo l'aumento della temperatura aumenta la tensione di vapore?
Poiché le molecole acquistano energia cinetica e superano più facilmente le forze intermolecolari, si verifica una maggiore evaporazione.
Perché l'acqua non è così volatile come l'acetone?
Gli elevati legami idrogeno dell'acqua richiedono più energia per essere spezzati e sono quindi meno volatili.
La pressione di vapore può prevedere la volatilità?
Sì. Una maggiore pressione di vapore indica una maggiore volatilità e un'evaporazione più rapida.
Perché la pressione di vapore è così importante per le previsioni meteorologiche?
Viene utilizzata per calcolare l'umidità, il punto di rugiada e la condensazione, essenziali per prevedere la pioggia e lo sviluppo delle nuvole.

 Bar
Bar
 Perline e sfere
Perline e sfere
 Bulloni e dadi
Bulloni e dadi
 Crogioli
Crogioli
 Dischi
Dischi
 Fibre e tessuti
Fibre e tessuti
 Film
Film
 Fiocco
Fiocco
 Schiume
Schiume
 Lamina
Lamina
 Granuli
Granuli
 Nidi d'ape
Nidi d'ape
 Inchiostro
Inchiostro
 Laminato
Laminato
 Grumi
Grumi
 Maglie
Maglie
 Film metallizzato
Film metallizzato
 Piatto
Piatto
 Polveri
Polveri
 Asta
Asta
 Lenzuola
Lenzuola
 Cristalli singoli
Cristalli singoli
 Bersaglio di sputtering
Bersaglio di sputtering
 Tubi
Tubi
 Lavatrice
Lavatrice
 Fili
Fili
 Convertitori e calcolatori
Convertitori e calcolatori
 Scrivi per noi
Scrivi per noi
 Chin Trento
Chin Trento



